Nghiên cứu gần đây đã đề xuất vai trò của hệ vi sinh vật đường ruột trong sinh bệnh học và khả năng điều trị một loạt các bệnh về gan. Hệ vi sinh vật đường ruột và các sản phẩm vi khuẩn có thể góp phần phát triển các bệnh về gan thông qua nhiều cơ chế bao gồm tăng tính thấm của ruột, viêm hệ thống mãn tính, sản xuất axit béo chuỗi ngắn và thay đổi quá trình trao đổi chất. Điều này cho thấy vai trò tiềm năng của các sản phẩm pre-, pro- và synbiotic trong việc phòng ngừa hoặc điều trị một số bệnh về gan. Ngoài ra, có bằng chứng mới nổi về tác động của việc cấy ghép vi sinh vật trong phân. Trong tài liệu này, chúng tôi thảo luận về mối quan hệ giữa hệ vi sinh vật đường ruột và các bệnh về gan, cũng như xem xét các lựa chọn điều trị dựa trên hệ vi sinh vật đường ruột hiện đang được nghiên cứu.
Những điểm chính:
- Hệ vi sinh vật đường ruột và các sản phẩm vi khuẩn có thể ảnh hưởng trực tiếp và gián tiếp đến gan thông qua các cơ chế khác nhau, dẫn đến nhiều loại bệnh về gan.
- Điều này cho thấy vai trò tiềm năng của các sản phẩm pre-, pro- và synbiotic trong việc phòng ngừa hoặc điều trị một số bệnh về gan.
- Ngoài ra còn có bằng chứng mới cho thấy việc cấy ghép hệ vi sinh vật trong phân có thể là một phương pháp điều trị hiệu quả đối với một số bệnh về gan.
Mục đích của đánh giá này là phác thảo cách IM và gan tương tác với nhau. Chúng tôi sẽ tập trung vào vai trò của IM trong cơ chế bệnh sinh và điều trị các bệnh về gan, đặc biệt là bệnh gan nhiễm mỡ không do rượu (NAFLD), bệnh gan liên quan đến rượu (ALD), viêm đường mật xơ cứng nguyên phát, viêm đường mật nguyên phát, ung thư biểu mô tế bào gan (HCC) và xơ gan. Đánh giá này sẽ tập trung vào dữ liệu lâm sàng và các biện pháp can thiệp cho từng bệnh lý này.
Hệ vi sinh vật đường ruột và bệnh gan: Cơ chế tổng thể
Chuyển hóa axit mật
Được tổng hợp từ cholesterol trong gan, axit mật (BA) rất cần thiết trong quá trình chuyển hóa cholesterol và tiêu hóa lipid. BA được lưu trữ trong túi mật và được tiết ra trong quá trình tiêu hóa ở ruột non. 95% BA được tái hấp thu ở đoạn cuối hồi tràng và vận chuyển trở lại gan qua tĩnh mạch cửa. BA thúc đẩy sự hấp thụ chất béo, cholesterol và vitamin tan trong chất béo trong chế độ ăn uống. Ngoài ra, BA còn có chức năng như các phân tử tín hiệu ảnh hưởng đến các quá trình sinh lý, bao gồm sự điều hòa chuyển hóa glucose và lipid thông qua kích hoạt thụ thể farnesoid X (FXR) và liên kết với thụ thể axit mật kết hợp G-protein 1. BA cũng có thể ảnh hưởng đến IM vì nó đã được chứng minh là có liên quan trực tiếp đến tính toàn vẹn của niêm mạc ruột và sự tổng hợp các peptide kháng khuẩn. Khi BA liên kết với FXR, các peptide kháng khuẩn, chẳng hạn như angiogenin 1, được tạo ra. Những peptide này có thể ức chế sự phát triển quá mức của IM bằng cách tăng tiềm năng tế bào biểu mô ruột để ngăn chặn sự hấp thu của vi khuẩn, cải thiện chức năng hàng rào ruột. Ngược lại, IM có thể ảnh hưởng đến quy mô và thành phần của nhóm BA thông qua việc chuyển đổi BA sơ cấp thành BA thứ cấp. Điều này sau đó có thể thay đổi thành phần của BA tuần hoàn, hoạt động như các phân tử tín hiệu ảnh hưởng, chẳng hạn như chuyển hóa lipid và glucose và khiến các cá nhân dễ mắc bệnh gan nhiễm mỡ không do rượu (NAFLD). Do đó, cả rối loạn sinh lý của IM và/hoặc mất cân bằng BA đều có thể góp phần vào cơ chế bệnh sinh và sự tiến triển của bệnh gan, điều này sẽ được thảo luận.
Tính thấm của ruột
Biểu mô ruột đóng vai trò thiết yếu trong việc hạn chế độc tố, kháng nguyên và hệ vi khuẩn đường ruột xâm nhập vào hệ tuần hoàn, đồng thời cho phép hấp thu có chọn lọc các chất dinh dưỡng qua các mối nối chặt chẽ. Hàng rào ruột bao gồm các tế bào ruột liên kết với nhau bằng các protein xuyên màng bao gồm desmosome, các điểm nối và các mối nối chặt chẽ. Hàng rào ruột cũng được củng cố nhờ các globulin miễn dịch, chất nhầy và vi khuẩn hội sinh. IM có thể làm thay đổi hàng rào ruột bằng cách thay đổi các mối nối chặt chẽ, làm suy giảm lớp chất nhầy hoặc ức chế sản xuất chất nhầy, sau đó làm tăng tính thấm của biểu mô.
Một cách mà IM có liên quan đến việc tăng tính thấm của mối nối chặt chẽ là thông qua sự hiện diện của nội độc tố trong lòng. Nội độc tố được tìm thấy trên màng ngoài của vi khuẩn gram âm làm tăng tính thấm của mối nối chặt chẽ bằng cách tăng biểu hiện thụ thể giống thu phí (TLR)4. Việc mở rộng các mối nối chặt chẽ dẫn đến tăng tính thấm của ruột, dẫn đến tăng sự di chuyển của các mảnh vi khuẩn và nội độc tố vào tuần hoàn cửa và sau đó là gan. Điều này có thể gây viêm gan, viêm hệ thống và tổn thương gan. Các mảnh và sản phẩm vi khuẩn cũng có thể huy động và kích hoạt các tế bào miễn dịch ở gan, góp phần hơn nữa vào sự tiến triển của bệnh gan.
Viêm mãn tính
IM góp phần gây ra tình trạng viêm mãn tính không chỉ thông qua việc sản xuất nội độc tố mà còn thông qua các cytokine và rối loạn chức năng gây viêm. Sự chuyển vị của nội độc tố có nguồn gốc từ IM vào hệ thống tuần hoàn làm tăng biểu hiện TLR4, kích hoạt các cytokine tiền viêm yếu tố hoại tử khối u-alpha (TNF-a) và interleukin (IL)-6, 26 do đó gây ra tình trạng viêm toàn . Inflammasomes, bao gồm các protein lặp lại giàu leucine và các miền liên kết với nucleotide, chi phối sự phân cắt của các cytokine tiền viêm. Rối loạn sinh học đã được chứng minh là có liên quan đến sự thiếu hụt hồng cầu, đặc biệt là NLRP 3 và 6, dẫn đến tăng biểu hiện TNF-a. Việc tăng cường kích hoạt và sản xuất TLR4 cũng như các cytokine tiền viêm do rối loạn sinh học cũng có thể dẫn đến việc huy động và kích hoạt các tế bào miễn dịch ở gan, góp phần vào sự tiến triển của bệnh gan.
Kích hoạt hệ thống miễn dịch
Việc huy động và kích hoạt các tế bào miễn dịch ở gan có thể được gây ra bởi các tín hiệu cục bộ hoặc tín hiệu từ các nguồn như IM. Hệ thống miễn dịch được chia thành hệ thống miễn dịch bẩm sinh và hệ thống miễn dịch thích nghi. Hệ thống miễn dịch bẩm sinh bảo vệ chống lại các vi sinh vật và độc tố, trong khi hệ thống miễn dịch thích nghi có đặc tính kháng nguyên và đòi hỏi khả năng tự nhận biết. Tế bào Kupffer (KC) là thành phần quan trọng của hệ thống miễn dịch bẩm sinh, cư trú trong khoang mạch hình sin. KC có thể được kích hoạt bởi nhiều kích thích nội sinh và ngoại sinh khác nhau bao gồm cả nội độc tố. Kích hoạt KC kích hoạt sản xuất các cytokine gây viêm, chẳng hạn như TNF-α, cũng như các loại oxy phản ứng (ROS) có thể gây tổn thương mô. Những cytokine này cũng có thể đóng một vai trò quan trọng trong việc điều chỉnh kiểu hình và chức năng của các tế bào nhu mô và không nhu mô lân cận. Ví dụ, các cytokine đã được chứng minh là có khả năng phân cực và kích hoạt kiểu hình M1 tiền viêm ở KC.
Tế bào diệt tự nhiên (NK) và tế bào diệt tự nhiên T (NKT) cũng có thể đóng vai trò trong cơ chế bệnh sinh của bệnh gan và có thể bị ảnh hưởng bởi IM. Các nghiên cứu gần đây trên chuột đã chỉ ra rằng các kháng nguyên có nguồn gốc từ IM có thể ảnh hưởng đến thành phần và hoạt hóa của tế bào NKT ở gan. Tế bào NK trong gan đóng vai trò liên kết phản ứng miễn dịch bẩm sinh và thích nghi. Các tế bào NK được kích hoạt đã được phát hiện là có tác dụng chống xơ hóa, bằng cách giải phóng interferon-γ (IFN-γ) gây ra hiện tượng ngừng chu kỳ tế bào hình sao ở gan (HSC) và gây chết tế bào.
Tuy nhiên, IFN-γ cũng gây ra apoptosis tế bào gan và do đó gây tổn thương gan. tế bào NKT, có thể được biểu hiện bởi tế bào gan và tế bào trình diện kháng nguyên, có chung đặc tính của cả tế bào T và tế bào NK. tế bào NKT có thể tiết ra các cytokine và do đó đóng vai trò quan trọng trong việc điều khiển hệ thống miễn dịch. Chúng có thể làm được điều này thông qua khả năng sản xuất tế bào T trợ giúp 1 có khả năng chống viêm và tế bào T trợ giúp 2 có khả năng chống viêm. Nhìn chung, việc kích hoạt các tế bào miễn dịch ở gan bằng IM có thể góp phần vào cơ chế bệnh sinh của một số bệnh về gan.
Axit béo chuỗi ngắn
Một cơ chế khác mà IM có thể góp phần gây ra bệnh gan là thông qua việc sản xuất axit béo chuỗi ngắn (SCFA). IM phá vỡ carbohydrate không tiêu hóa được và giải phóng SCFA trong ruột người. SCFA chính là acetate, propionate và butyrate, được chuyển hóa lần lượt ở cơ, gan và biểu mô. Nghiên cứu chủ yếu tập trung vào butyrate, nguồn năng lượng chính cho tế bào ruột kết, giúp cải thiện chức năng hàng rào đại tràng và do đó tác động tích cực đến tính thấm của ruột. Butyrate đã được chứng minh là cải thiện hàng rào ruột bằng cách tạo ra các protein và chất nhầy có mối nối chặt chẽ, đặc biệt là Mucin 2 và tăng cường biểu hiện claudin-1. Ở gan, butyrate có thể gây ra apoptosis và có thể ức chế sự tăng sinh tế bào trong tế bào gan bằng cách ức chế biểu hiện sirtuin1 trong khi điều chỉnh tăng biểu hiện miR-22. Do đó, butyrate cũng có thể ức chế tế bào ung thư gan. Butyrate cũng đã được chứng minh là làm tăng cảm giác no, giảm lượng thức ăn ăn vào và trì hoãn quá trình làm rỗng dạ dày thông qua kích hoạt thụ thể axit béo tự do 3. Thụ axit béo tự do 3 điều chỉnh tăng cường sản xuất hormone đường ruột peptide YY và peptide giống glucagon-1. Do đó, IM có thể ảnh hưởng đến quá trình trao đổi chất, bao gồm cả bệnh béo phì do chế độ ăn kiêng.
Cuối cùng, butyrate cũng có thể tác động đến tình trạng viêm. Trong đường ruột, các nghiên cứu đã phát hiện ra rằng butyrate liên kết và kích hoạt gamma thụ thể kích hoạt peroxisome proliferator kích hoạt (PPAR-y), đối kháng với sự tải nạp yếu tố hạt nhân-kappa B (NF-kB), do đó gây ra tác dụng chống viêm. Do đó, sự hiện diện và/hoặc lượng butyrate dồi dào do IM tạo ra có thể tác động đến cơ chế bệnh sinh của bệnh gan thông qua một số cơ chế.
Cholin
Choline là một chất dinh dưỡng thiết yếu và là thành phần phospholipid của màng tế bào, có thể được chuyển hóa bằng IM. Có một số cơ chế mà qua đó sự thiếu hụt choline có thể ảnh hưởng đến gan, bao gồm sự hình thành lipoprotein mật độ rất thấp (VLDL), rối loạn chức năng ty thể và căng thẳng mạng lưới nội chất. Phosphatidylcholine, là một phospholipid có chứa choline ở nhóm đầu, là thành phần chính của vỏ VLDL. Thiếu choline, do chế độ ăn uống hoặc do chuyển hóa IM, dẫn đến giảm hình thành VLDL và xuất khẩu chất béo trung tính từ gan, dẫn đến phát triển gan nhiễm mỡ. Choline cũng là một thành phần thiết yếu của màng ty thể. Sự thiếu hụt choline làm giảm nồng độ màng ty thể của phosphatidyletanolamine và phosphatidylcholine, dẫn đến giảm điện thế màng, từ đó gây ra tổn thương oxy hóa.
IM có thể góp phần làm giảm khả dụng sinh học của choline46 cách chuyển hóa choline trong chế độ ăn uống có trong trứng, sữa và thịt đỏ thành trimethylamine (TMA). Điều này làm tăng sản xuất TMA, chất này được hấp thụ vào máu và có liên quan đến việc tăng nguy cơ mắc bệnh tim mạch. Ngoài ra, một khi TMA đến gan, nó sẽ được chuyển hóa thêm bởi monooxygenase 1 và 3 chứa flavin để tạo ra trimethylamine-N-oxide (TMAO). Điều này có thể dẫn đến tăng tích lũy chất béo trung tính ở gan do TMAO ảnh hưởng đến kích thước nhóm BA bằng cách giảm tổng hợp BA thông qua việc ức chế các enzyme chủ chốt và bằng cách hạn chế sự lưu thông trong gan của BA thông qua việc ức chế chất vận chuyển anion hữu cơ và biểu hiện protein gia đình đa kháng thuốc. Do đó, có thể thiếu choline, thông qua chế độ ăn uống hoặc chuyển đổi IM thành TMA, có thể khiến chất béo tích tụ trong gan.
Ethanol
Ethanol, chủ yếu có trong thực phẩm và đồ uống, được hấp thụ qua niêm mạc đường tiêu hóa. Tuy nhiên, ethanol cũng có thể được sản xuất và chuyển hóa bởi IM khi không tiêu thụ rượu. Ethanol được hình thành từ Escherichia coli và trong điều kiện yếm khí trong quá trình lên men carbohydrate, E. coli có thể chuyển hóa axit pyruvic để tạo ra acetaldehyde, chất này có thể bị khử thành ethanol. Acetaldehyde đã được chứng minh là làm giảm chức năng hàng rào ruột bằng cách làm suy yếu các mối nối chặt chẽ và do đó tạo điều kiện thuận lợi cho việc di chuyển các sản phẩm vi sinh vật vào hệ tuần hoàn. Hơn nữa, các nghiên cứu đã chỉ ra rằng acetaldehyde có thể kích thích phản ứng miễn dịch viêm và thích ứng bằng cách điều hòa giảm biểu hiện peptide kháng khuẩn trong ruột, do đó dẫn đến nhiều tác dụng phụ hơn nữa. tổn thương gan.
Khi kết hợp với nhau, IM và các sản phẩm vi khuẩn có thể ảnh hưởng trực tiếp và gián tiếp đến gan thông qua nhiều cơ chế khác nhau (Hình 1), dẫn đến nhiều loại bệnh về gan (Hình 2).
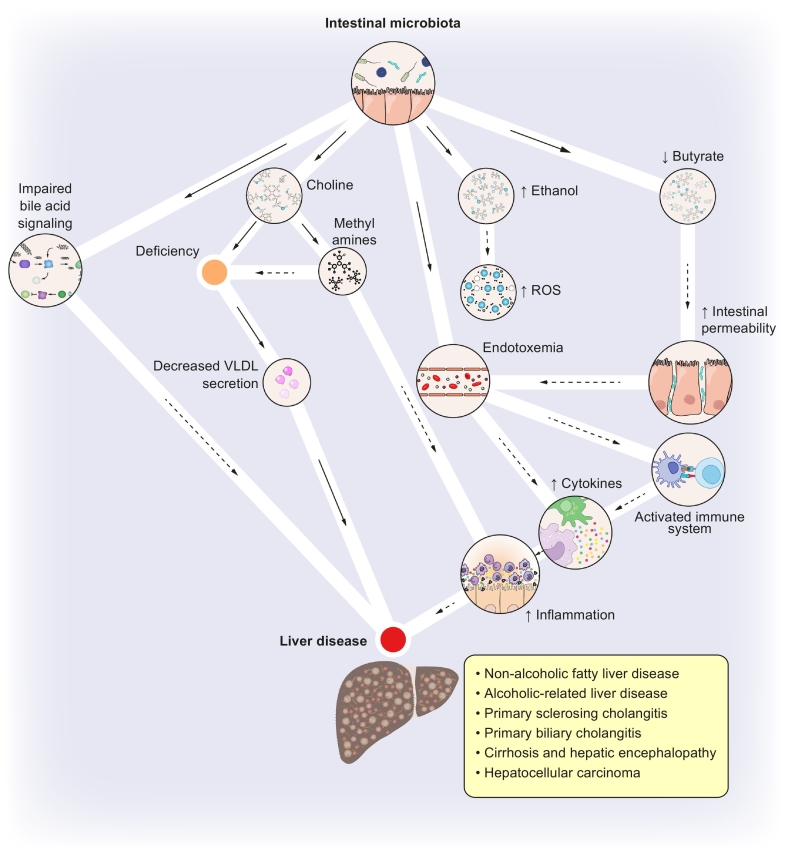
Hình 1: Cơ chế mà hệ vi sinh vật đường ruột có thể ảnh hưởng đến gan. ROS, loại oxy phản ứng; VLDL, lipoprotein mật độ rất thấp.
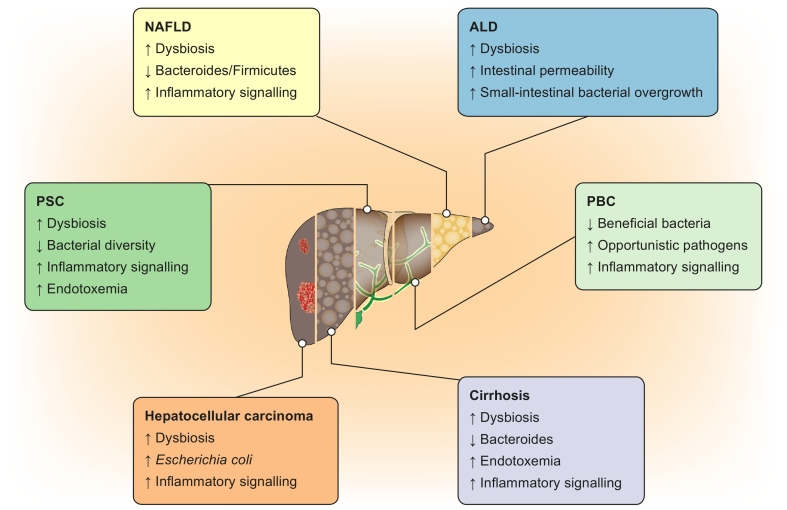
Hình 2: Vai trò của hệ vi sinh vật đường ruột trong bệnh gan.
ALD, bệnh gan do rượu; NAFLD, bệnh gan nhiễm mỡ không do rượu; PBC, viêm đường mật nguyên phát; PSC có nghĩa là Viêm đường mật xơ cứng nguyên phát.
Vi khuẩn đường ruột và các bệnh gan cụ thể
Bệnh gan nhiễm mỡ không do rượu
NAFLD là một trong những nguyên nhân phổ biến nhất gây ra bệnh gan trên toàn thế giới, ảnh hưởng đến 15–30% dân số nói chung. NAFLD dao động từ sự lắng đọng chất béo đơn giản trong gan (nhiễm mỡ) đến viêm (viêm gan nhiễm mỡ không do rượu hoặc NASH) đến xơ hóa và xơ gan. Các nghiên cứu đã chỉ ra rằng thành phần IM bị thay đổi, được gọi là “rối loạn sinh học”, góp phần vào cơ chế bệnh sinh của NAFLD, tuy nhiên mối quan hệ nhân quả vẫn chưa được chứng minh.
Mặc dù có số lượng lớn dữ liệu tiền lâm sàng điều tra và chứng minh mối quan hệ giữa rối loạn sinh học và NAFLD, nhưng chỉ có một số nghiên cứu hạn chế ở người, hầu hết là cắt ngang, đã điều tra vai trò của IM trong NAFLD, với các kết quả khác nhau. Ở người lớn, bệnh nhân mắc NASH được phát hiện có lượng Bacteroidetes thấp hơn, không phụ thuộc vào chỉ số khối cơ thể và chế độ ăn uống. Các nghiên cứu đã chỉ ra rằng có sự khác biệt về IM giữa bệnh nhân mắc NAFLD và người đối chứng khỏe mạnh. Một nghiên cứu cho thấy mức độ nghiêm trọng của NAFLD có liên quan đến rối loạn sinh lý IM và sự thay đổi chức năng trao đổi chất của IM. Cụ thể, họ phát hiện ra rằng sự phong phú của Bacteroides có liên quan độc lập với NASH và Ruminococcus với bệnh xơ hóa. Gần đây hơn, một nghiên cứu cắt ngang khác cho thấy những người mắc NAFLD đã giảm đáng kể Bacteroidetes và Firmicutes , cùng với lượng Lactobacillus tăng lên so với nhóm đối chứng khỏe mạnh, trong khi những người mắc NASH đã giảm Ruminococcus, Faecalibacter prausnitzii và Coprococcus so với nhóm đối chứng khỏe mạnh, độc lập với cơ thể. chỉ số khối và tình trạng kháng insulin. Trong nhi khoa, kết quả cho thấy lượng E. coli tăng lên ở bệnh nhân mắc NASH so với nhóm đối chứng khỏe mạnh, điều này có liên quan đến nồng độ cồn trong máu cao hơn. Một nghiên cứu can thiệp, bao gồm 15 phụ nữ trưởng thành áp dụng chế độ ăn thiếu choline, đã phát hiện ra rằng thành phần hệ vi sinh vật trước khi ăn kiêng, đặc biệt là lượng Gammaproteobacteria dồi dào thấp hơn hoặc lượng Erysipelotrichi dồi dào hơn làm tăng nguy cơ phát triển gan nhiễm mỡ trong quá trình suy giảm choline. nữa, họ phát hiện ra rằng kiểu gen của vật chủ (đa hình đơn nucleotide trong gen PEMT ) và IM cụ thể có thể dự đoán gan nhiễm mỡ do thiếu choline (được đánh giá bằng hình ảnh cộng hưởng từ). Một nghiên cứu đã đánh giá các hợp chất hữu cơ dễ bay hơi ester trong phân và phát hiện ra rằng các mẫu cụ thể có liên quan đến sự khác biệt trong IM khi bệnh nhân mắc NAFLD, được chẩn đoán trên siêu âm, được so sánh với nhóm đối chứng. Gần đây, một nghiên cứu điều tra mối quan hệ giữa IM và chức năng miễn dịch ở NAFLD đã phát hiện ra rằng các tế bào miễn dịch cụ thể ở vùng cửa hoặc tiểu thùy có tương quan với IM cụ thể trong phân. Cụ thể Faecalibacter prausnitzii có tương quan nghịch với CD45 + và CD163 +tế bào ở đường cửa và Prevotella có tương quan nghịch với tế bào CD20 + ở tiểu thùy gan. Tổng hợp lại, một số nghiên cứu đã cho thấy mối liên hệ giữa IM hoặc các sản phẩm vi khuẩn và NAFLD.
Bệnh gan do rượu
ALD xảy ra ở những bệnh nhân lạm dụng rượu thường xuyên. Giống như NAFLD, ALD không tiến triển được đặc trưng bởi sự tích tụ chất béo trong gan, trong khi ALD tiến triển (viêm gan nhiễm mỡ do rượu) biểu hiện viêm gan. Gần đây, nghiên cứu đã điều tra vai trò của IM trong ALD, đặc biệt tập trung vào việc rượu có thể gây ra chứng rối loạn sinh lý liên quan đến hệ vi sinh vật như thế nào, từ đó có thể góp phần vào cơ chế bệnh sinh của ALD.
Nhiều nghiên cứu ở cấp độ tiền lâm sàng và thực nghiệm đã làm sáng tỏ mối quan hệ giữa ALD và chứng rối loạn sinh lý. Thông qua nhiều nghiên cứu này, nhiều mầm bệnh, thành phần độc hại và con đường đã được chứng minh là có liên quan đến sự phát triển của ALD. Rất tiếc, lượng dữ liệu lâm sàng không được nhiều.
Các nghiên cứu bao gồm cả mô hình chuột và người tham gia đã phát hiện ra rằng việc tiêu thụ rượu gây ra sự thay đổi trong IM dẫn đến rối loạn sinh lý. Cụ thể, bệnh nhân mắc ALD có nồng độ Bifidobacteria , Enterobacter và Lactobacillus spp thấp hơn, trong khi bệnh nhân xơ gan mắc ALD biểu hiện giảm đáng kể Bacteroidetes và Firmicutes ngành. Mặt khác, Proteobacteria, Fusobacteria và Actinobacteria phyla lại tăng lên. Các nghiên cứu khác sử dụng mẫu phân của bệnh nhân nghiện rượu cho thấy lượng Lactobacillus spp. giảm, trong khi bệnh nhân xơ gan được chứng minh là có lượng Bifidobacteria spp.. trong phân thấp hơn. Khi so sánh IM của người nghiện rượu từ xơ gan đến nghiện rượu không xơ gan, người ta thấy rằng IM của những người bị xơ gan chứa nhiều Enterobactericeae hơn. Dựa trên một số phát hiện này, thuật ngữ tỷ lệ rối loạn sinh lý xơ gan (CDR) đã được đề xuất, đại diện cho tỷ lệ vi khuẩn tự thân hoặc vi khuẩn có lợi so với vi khuẩn có khả năng gây bệnh, với tỷ lệ thấp tương quan với bệnh tiến triển hơn tình trạng. So với các nguyên nhân gây xơ gan khác, ALD có tỷ lệ thấp nhất.
Các nghiên cứu cũng chứng minh sự gia tăng tổng số lượng vi sinh vật trong ruột non của bệnh nhân nghiện rượu. Một đánh giá về người nghiện rượu mãn tính so với bệnh nhân không có tiền sử lạm dụng rượu, sử dụng xét nghiệm hơi thở hydro, cho thấy tỷ lệ vi khuẩn đường ruột phát triển quá mức (SIBO) ở người nghiện rượu cao hơn đáng kể so với điều khiển. Tuy nhiên, không có sự khác biệt được tìm thấy giữa bệnh nhân nghiện rượu bị xơ gan và những người không bị xơ gan. Sự hiện diện của SIBO đã được chứng minh là có mối tương quan đáng kể với tỷ lệ viêm phúc mạc tự phát do vi khuẩn cao hơn và với mức độ nghiêm trọng của bệnh xơ gan do rượu. Những thay đổi trong IM của bệnh nhân nghiện rượu dường như đi kèm với những thay đổi về pH đại tràng và gan nhiễm mỡ. Nó cũng tương quan với mức độ nội độc tố trong huyết thanh cao hơn và mức độ TNF-α trong ruột tăng lên, cũng như mức độ oxit nitric, IL-6 và IL-8 tăng lên. Các nghiên cứu khác cũng tìm thấy hàm lượng các sản phẩm vi khuẩn trong máu của bệnh nhân nghiện rượu cao hơn so với nhóm đối chứng khỏe mạnh. Ngoài ra, nhiễm độc nội độc tố sau khi nhiễm độc rượu cấp tính đã được chứng minh là có liên quan đến rối loạn huyết động trong tăng huyết áp cổng thông tin do xơ gan. Những phát hiện này cho thấy mối liên hệ tiềm ẩn giữa rối loạn sinh lý và ALD, với việc rượu thúc đẩy rối loạn sinh lý và dẫn đến tăng tính thấm của hàng rào ruột, do đó gây ra sự dịch chuyển của IM và nội độc tố vào tuần hoàn cửa và cuối cùng là gan . Điều này lại gây ra tình trạng viêm gan và tổn thương gan, đặc biệt thông qua sự tương tác giữa lipopolysacarit (LPS) và TLR.
Viêm đường mật xơ cứng nguyên phát
Viêm đường mật xơ cứng nguyên phát (PSC) được đặc trưng bởi tình trạng viêm và sẹo của ống mật. Một số nghiên cứu điều tra IM ở PSC đã cho thấy sự suy giảm tổng thể về tính đa dạng của IM, tuy nhiên, có sự mâu thuẫn trong những phát hiện này ở cấp độ chi và loài.
Việc đánh giá IM ở bệnh nhân mắc PSC và bệnh viêm ruột PSC (IBD) cho thấy tính đa dạng vi khuẩn thấp, và sự biểu hiện quá mức của các giống Rothia , Enterococcus, Streptococcus , Clostridium , Veillonella , Haemophilus , Fusobacteria và Lactobacillus bất kể IBD đi kèm. Một nghiên cứu khác xác nhận rằng sự phong phú của Veillonella đã tăng lên rõ rệt ở PSC so với nhóm đối chứng khỏe mạnh. Các nghiên cứu xem xét sinh thiết đường ruột cho thấy hồ sơ hệ vi sinh vật tổng thể của những người mắc PSC được đặc trưng bởi sự phong phú của Barnesiellaceae và giảm Clostridiales.
Theo các nghiên cứu đã nói ở trên, những thay đổi này dẫn đến rối loạn sinh lý IM và có liên quan đến cơ chế bệnh sinh của PSC bằng cách tạo ra vi khuẩn, từ đó kích hoạt con đường tiền viêm trong tế bào cholangiocytes dẫn đến xơ hóa và viêm. Vi khuẩn cũng có thể đóng một vai trò trong việc bắt chước phân tử, thông qua nội độc tố, dẫn đến việc tạo ra các kháng thể và gây tổn thương đường mật qua trung gian miễn dịch.
Viêm đường mật nguyên phát
Viêm đường mật nguyên phát (PBC) là một bệnh dẫn đến sự phá hủy dần dần các ống mật trong gan. Trong một nghiên cứu cắt ngang so sánh những bệnh nhân chưa từng điều trị bằng axit urodeoxycholic (UDCA) với PBC và những người đối chứng khỏe mạnh, chứng rối loạn sinh học đã được quan sát thấy ở PBC và được UDCA đảo ngược một phần. Bacteroidetes spp. đã giảm đáng kể và Fusobacteria, Haemophilus, Veillonella, Clostridium, Lactobacillus, Streptococcus, Pseudomonas, Klebsiella, một chi chưa được biết đến trong họ Enterobacteriaceae và Proteobacteria spp. được đại diện quá mức so với các biện pháp kiểm soát lành mạnh. Một nghiên cứu khác so sánh bệnh nhân mắc PBC với nhóm đối chứng khỏe mạnh cho thấy bệnh nhân mắc PBC đã suy giảm lượng vi khuẩn đường ruột có lợi, bao gồm Acidobacteria, Lachnobacteria spp., Bacteroides eggerthii và Ruminococcus bromii , nhưng mức độ phân loại vi khuẩn chứa mầm bệnh cơ hội cao hơn, chẳng hạn như y -Proteobacteria, Enterobacteriaceae , Neisseriaceae , Spirochaetaceae , Veillonella , Streptococcus , Klebsiella , Actinobacillus pleuropneumoniae , Anaeroglobus geminatu s, Enterobacter asburiae , Haemophilus parainfluenzae , Megasphaera micronuciformis và Paraprevotella clara. Họ cũng phát hiện ra rằng sự thay đổi liên quan đến PBC trong IM này có liên quan đến việc tăng các chỉ số tổn thương gan và các cytokine gây viêm trong huyết thanh, do đó gợi ý rằng IM bị thay đổi có thể liên quan đến sự khởi phát hoặc phát triển của PBC.
Các cơ chế tiềm ẩn liên quan đến IM đằng sau sự tiến triển của bệnh gan tương tự như các cơ chế đã nói ở trên được mô tả trước đây đối với PSC.
Xơ gan và bệnh não gan
Xơ gan được coi là bệnh gan giai đoạn cuối với đặc điểm là xơ hóa nặng và mất tế bào gan. Mỗi bệnh gan nói trên đều có thể dẫn đến xơ gan. Nghiên cứu đã phát hiện ra rằng bệnh nhân xơ gan có lượng Bacteroidetes thấp hơn và lượng Proteobacteria , Enterococcus, Veillonella, Megasphaera, Burkholderia, Prevotella và Fusobacteria cao hơn. Ngoài ra, bệnh nhân xơ gan còn có mức taxa tự thân thấp hơn như Blautia, Roseburia, Faecalibacerium, Dorea, Lachnospiraceae và Ruminococcaceae. Khi phân tích hệ vi sinh vật niêm mạc tá tràng của 30 bệnh nhân xơ gan, Chen et al. phát hiện ra rằng sự xâm chiếm của bệnh nhân xơ gan khác biệt đáng kể so với 28 đối chứng khỏe mạnh.
Dường như có sự hiện diện quá mức của Veillonella , Megasphaera , Dialister , Atopobium và Prevotella ở bệnh nhân xơ gan so với nhóm chứng. Veillonella , Prevotella, Neisseria và Haemophilus là những loài có khả năng phân biệt tốt nhất giữa những người bị xơ gan và những người khỏe mạnh. Các nghiên cứu khác đã chứng minh mức độ cao hơn của hệ vi sinh vật có nguồn gốc từ miệng trong mẫu phân của bệnh nhân xơ gan, cũng như hệ vi sinh vật nước bọt bị thay đổi đáng kể ở bệnh nhân xơ gan. Điều này có thể gợi ý rằng hệ vi sinh vật đường miệng có tác động lớn đến hệ vi sinh vật đường ruột và tá tràng ở nhóm đối tượng này. Một tác giả khác thậm chí còn đề cập đến khả năng hệ vi sinh vật tá tràng có thể trực tiếp góp phần gây ra bệnh não gan ở bệnh xơ gan.
Bệnh não gan, được định nghĩa là suy giảm nhận thức, xảy ra do bệnh gan nặng. Các nghiên cứu đã phát hiện ra rằng có mối liên hệ giữa bệnh não gan và các sản phẩm phụ của IM, đặc biệt là nhiễm độc nội độc tố trong máu. Một nghiên cứu đã so sánh IM ở bệnh nhân mắc bệnh não gan với các bệnh nhân xơ gan khác và những người đối chứng khỏe mạnh và phát hiện ra rằng những người mắc bệnh não gan có nồng độ Alcaligenaceae, Enterobacteriaceae và Fusobacteriaceae cao hơn cùng với Ruminococcaceae và Lachnospiraceae thấp hơn. Trong số đó, Alcaligenaceae và Porphyromonadaceae có mối tương quan tích cực với suy giảm nhận thức trong khi Prevotella có liên quan đến việc cải thiện nhận thức và giảm viêm.
Nghiên cứu của họ cũng cho thấy nồng độ Veillonellaceae cao hơn, nhiễm độc nội độc tố và tình trạng viêm ở bệnh nhân mắc bệnh não gan. Một nghiên cứu khác chứng minh rằng thành phần của IM có thể dự đoán tình trạng mất bù và nhập viện của bệnh nhân xơ gan. Nồng độ nội độc tố trong huyết thanh cao hơn, CDR thấp hơn và các nhóm mầm bệnh tăng lên có liên quan đáng kể đến tử vong thứ phát do suy đa cơ quan khi so sánh với những bệnh nhân sống sót. Trong cùng một nghiên cứu, hệ vi sinh vật trong nước bọt đã được chứng minh là có mối tương quan độc lập với thời gian nằm viện 90 ngày liên quan đến gan bất kể mô hình điểm số bệnh gan giai đoạn cuối (MELD) hay tình trạng bệnh não gan.
Một số cơ chế đã được đề xuất về mối liên quan giữa IM và xơ gan bao gồm tăng tính thấm của ruột non và giảm nhu động ruột non, dẫn đến sự phát triển quá mức của ruột non. Điều này dẫn đến sự chuyển vị trí của IM và nội độc tố vào hệ tuần hoàn cửa, kích hoạt các con đường gây viêm trong HSC thông qua TLR4 và sau đó là sự phát triển của xơ hóa. Đối với HE, amoniac đóng vai trò trung tâm trong sự phát triển của bệnh. Một số nghiên cứu đã chỉ ra rằng ở những bệnh nhân bị xơ gan, ngoài sự di chuyển vi khuẩn và kích hoạt các cytokine tiền viêm, còn có sự gia tăng số lượng vi khuẩn hoạt động urease, dẫn đến tăng sản xuất amoniac ở ruột non và tăng nồng độ trong máu cửa.
Ung thư biểu mô tế bào gan
HCC có thể là biến chứng của nhiều bệnh về gan. Rối loạn sinh học có thể góp phần gây bệnh HCC bằng cách làm tăng tình trạng nhiễm mỡ, stress oxy hóa và viêm.
Những thay đổi trong hệ vi sinh vật bị nghi ngờ có vai trò trong quá trình gây ung thư. Một nghiên cứu của Grat et al. đã nghiên cứu IM của 15 bệnh nhân mắc HCC được ghép gan và so sánh họ với 15 bệnh nhân không mắc HCC nhưng có nguyên nhân tương tự của bệnh xơ gan và giai đoạn MELD tương tự. Nghiên cứu cho thấy sự hiện diện của HCC có liên quan đáng kể đến sự gia tăng Escherichia coli trong phân. Một nghiên cứu khác đánh giá các mẫu mô gan ở bệnh nhân mắc HCC và tìm thấy sự hiện diện của Helicobacter spp., cho thấy sự chuyển vị trong ruột là một cơ chế tiềm ẩn gây ung thư. Tuy nhiên, Helicobacter không thể được tìm thấy ở những bệnh nhân bị HCC do virus gây ra.
Về mặt cơ học, các nghiên cứu trên chuột cho thấy IM có thể góp phần vào sinh bệnh học HCC thông qua sự tương tác của nó với TLR, đặc biệt là TLR4. Tuy nhiên, cần nhiều nghiên cứu lâm sàng hơn để mô tả rõ hơn vai trò nguyên nhân của IM trong cơ chế bệnh sinh của HCC.
Những hạn chế đối với nghiên cứu bệnh IM và gan
Nghiên cứu trong lĩnh vực IM và bệnh gan đang phát triển nhanh chóng, nhưng có một số hạn chế cần cân nhắc khi giải thích mối liên quan này. Trước hết, những khác biệt về di và các yếu tố môi trường như chế độ ăn uống, và việc sử dụng thuốc/kháng sinh122 được chứng minh là góp phần tạo nên những biến đổi trong IM Ngoài ra, việc sử dụng các công cụ chẩn đoán gan khác nhau được sử dụng cho các mục tiêu chính trong các thử nghiệm lâm sàng cũng là một hạn chế khác.
Một số nghiên cứu sẽ sử dụng sinh thiết gan, tiêu chuẩn vàng để chẩn đoán, trong khi những nghiên cứu khác sử dụng các công cụ không xâm lấn và kém tin cậy hơn như chụp ảnh hoặc xét nghiệm máu, có thể giải thích những khác biệt được thấy trong nghiên cứu lâm sàng. Một hạn chế khác trong nghiên cứu IM ở người là cách thu thập mẫu phân.
Mặc dù ngành IM tương tự chiếm ưu thế ở dạ dày, ruột non và ruột kết, nhưng có sự khác biệt về thành phần và mức độ phong phú của IM. Phần lớn các nghiên cứu ở người phân tích mẫu phân, tuy nhiên 1 nghiên cứu đã tìm thấy sự khác biệt trong IM khi so sánh mẫu phân với thành phần trong manh tràng, do đó hạn chế tính tổng quát của kết quả. Hơn nữa, có những biến thể trong phương pháp giải trình tự được sử dụng, tất cả đều tạo ra những kết quả khác nhau. Chúng bao gồm PCR định lượng, giải trình tự 16S rRNA hoặc giải trình tự ngắn. Ngoài ra, sự khác biệt trong các nền tảng phân tích tin sinh học, chẳng hạn như QIIME, Mothur và PICRUST, có thể góp phần tạo nên sự khác biệt trong kết quả.
Nhìn chung, điều quan trọng là phải xem xét những hạn chế này khi phân tích nghiên cứu bệnh IM và bệnh gan cũng như chúng cần được xem xét khi thiết kế các nghiên cứu trong tương lai.
Định hướng tương lai
Dựa trên các nghiên cứu trên, có khả năng có mối liên quan giữa IM và bệnh gan, nhưng mối quan hệ nhân quả vẫn chưa được xác nhận. Một số nghiên cứu xem xét tác động của thao tác IM bằng pre-, pro- và synbiotic, cũng như cấy ghép hệ vi sinh vật trong phân (FMT), cho thấy rằng IM có vai trò trong các bệnh về gan.
Điều trị trước và bằng probiotic
Một số nghiên cứu đã nghiên cứu vai trò của việc điều trị trước và điều trị bằng men vi sinh ở bệnh nhân mắc bệnh gan. Một bản tóm tắt của những nghiên cứu này có thể được tìm thấy trong Bảng 1. Tuy nhiên, chưa có nghiên cứu nào được thực hiện ở bệnh nhân mắc PSC hoặc PBC.
Bảng 1
Tóm tắt các nghiên cứu về bệnh gan trước, ủng hộ và synbiotic.
| Bệnh | Sự đối đãi | Thiết kế nghiên cứu | kết quả | Thẩm quyền giải quyết |
| NAFLD | VSL#3 (sự kết hợp của 8 chủng probiotic) hoặc giả dược trong 4 tháng | RCT n = 48 trẻ | VSL#3 cải thiện NAFLD | 128 |
| NAFLD | Sản phẩm đa probiotic hoặc giả dược | RCT n = 58 người lớn | Probiotic dẫn đến giảm AST, GGT, TNF-a và IL-6 | 129 |
| NAFLD | Synbiotic hoặc giả dược | RCT n = 50 | Nhóm Synbiotic giảm đáng kể AST, cholesterol toàn phần, triacylglycerol và nhiễm mỡ (dựa trên Fibroscan) | 130 |
| ALD | Bifidobacteria bifidum và Pacobacillus plantarum hàng ngày trong 5 ngày | Nhãn mở ngẫu nhiên n = 66 | Giảm AST và ALT | 85 |
| ALD | Bifidobacteria bifidum, Bifidobacteria lactis, Bifidobacteria ongum, Lactobacillus acidophilus, Lactobacillus rhamnosus GG , Streptococcus thermophiles 5×10 9 1 viên hai lần mỗi ngày trong 28 ngày hoặc giả dược | RCT mù đôi n = 50 | SIBO giảm nhưng không có sự khác biệt về tính thấm của ruột | 131 |
| ALD/HE | VSL#3 hoặc giả dược | RCTl n = 130 | Không có sự khác biệt về tỷ lệ mắc bệnh não hoặc tỷ lệ tử vong. Tuy nhiên, đã thấy giảm Child-Pugh, MELD, TNF-a huyết tương, IL-1B và IL-6 | 132 |
| ALD/Xơ gan | Lactobacillus subtilis và Streptococcus faecium (hàng ngày trong 7 ngày) hoặc giả dược | RCT mù đôi n = 117 | Giảm TNF-a và tăng nồng độ albumin. Ổn định nồng độ LPS ở bệnh nhân xơ gan | 133 |
| ALD/Xơ gan | Lactobacillus casei Hirota (6,5×10 9 ) ba lần một ngày trong 4 tuần | Nhãn mở n = 12 | Khả năng thực bào bạch cầu trung tính được bình thường hóa. Không cải thiện khả năng kiểm soát bệnh và không thay đổi TNF-a, IL10 | 134 |
| ALD/Xơ gan | VSL#3 1 gói mỗi ngày trong 60 ngày hoặc giả dược | RCT mù đôi n = 63 | Giảm gradient áp lực gan tĩnh mạch và TNF-a | 135 |
| ALD/Xơ gan | VSL#3 2 gói 2 lần/ngày trong 60 ngày | Nghiên cứu thí điểm mở n = 8 | Xu hướng giảm nồng độ nội độc tố và TNF-a | 136 |
| ALD/Xơ gan | VSL #3 2 gói 2 lần mỗi ngày trong 60 ngày hoặc giả dược | RCT mù đôi n = 11 ALD và n = 15 xơ gan | Không tác động lên IM, nội độc tố, chức năng gan, áp lực gan tĩnh mạch. Giảm aldosterone huyết tương. | 137 |
| Xơ gan/HE | Lactobacillus rhamnosus GG hai lần mỗi ngày trong 8 tuần hoặc giả dược | RCT n = 30 | Không có sự thay đổi trong nhận thức. Tuy nhiên, giảm nội độc tố và TNF-a. | 138 |
| Xơ gan/HE | VSL#3 1 viên ba lần một ngày trong 3 tháng hoặc giả dược | RCT n = 86 | Giảm amoniac, SIBO và OCTT. Tăng điểm HE tâm lý và ngưỡng CFF. Ít hơn đáng kể bệnh nhân phát triển HE. | 139 |
| Xơ gan | Escherichia coli Nissle trong 42 ngày | RCT mù đôi n = 39 | Cải thiện sự xâm chiếm của ruột. Giảm nội độc tố và cải thiện chức năng gan/điểm Child-Pugh. | 140 |
| Xơ gan/HE | Lactulose và lactitol | Tổng quan Cochrane về các thử nghiệm đối chứng ngẫu nhiên n = 1828 | Tác dụng có lợi của disacarit không hấp thụ đối với tỷ lệ tử vong, HE, giảm các tác dụng phụ nghiêm trọng liên quan đến bệnh gan (suy gan, hội chứng gan, xuất huyết do giãn tĩnh mạch) | 141 |
| Xơ gan/HE | Bifidobacteria longum cộng với fructo-oligosaccharides trong 90 ngày hoặc giả dược | RCT mù đôi n = 60 | Giảm amoni (NH 4 ) và hiệu suất trong Thử nghiệm chế tạo thử nghiệm A và B. Cải thiện đáng kể thử nghiệm phương thức chữ số ký hiệu, thiết kế khối và MMSE | 142 |
| Xơ gan/HE | Điều trị Synbiotic hàng ngày trong 30 ngày hoặc giả dược | RCT n = 55 | Tăng Lactobacillus trong phân. Giảm nội độc tố, amoniac trong máu và đảo ngược HE tối thiểu ở 50%. Lớp Child-Pugh cải thiện 50%. | 143 |
ALD, bệnh gan do rượu; ALT, alanine aminotransferase; AST, aspartate aminotransferase; CFF, tần số nhấp nháy tới hạn; GGT, gamma-glutamyl transferase; HE, bệnh não gan; IL-, interleukin-; IM, hệ vi sinh vật đường ruột; LPS, lipopolysacarit; MELD, mô hình bệnh gan giai đoạn cuối; MMSE, kiểm tra trạng thái tinh thần tối thiểu; NAFLD, bệnh gan nhiễm mỡ không do rượu; OCTT, thời gian vận chuyển nội địa; RCT, thử nghiệm ngẫu nhiên có đối chứng; SIBO, vi khuẩn ruột non phát triển quá mức; TNF-a, yếu tố hoại tử khối u-alpha.
Nhìn chung, pre-, pro- và synbiotic dường như cải thiện các thông số gan khác nhau ở bệnh nhân NAFLD, ALD, xơ gan hoặc HE, hỗ trợ vai trò của IM trong bệnh lý bệnh gan. Tuy nhiên, các biện pháp can thiệp khác nhau về loại sản phẩm và số lượng sử dụng và hầu hết các nghiên cứu đều có cỡ mẫu nhỏ. Do đó, cần có nhiều nghiên cứu hơn với các thử nghiệm ngẫu nhiên có đối chứng lớn hơn trước khi đưa ra bất kỳ khuyến nghị nào. Câu trả lời có thể đến từ các thử nghiệm lâm sàng hiện đang được tiến hành; để biết các nghiên cứu hiện đang tuyển dụng, hãy xem bảng 2.
Bảng 2
Đang tiến hành thử nghiệm trước, ủng hộ và synbiotic.
| Loại bệnh gan | Loại pre-, pro hoặc synbiotic | Thiết kế nghiên cứu | Kết quả chính | Vị trí | ID lâm sàngTrial.gov |
| NAFLD | 2x men vi sinh/ngày: Lactobacillus acidophilus 1×10 9 CFU + Bifidobacteria lactis 1×10 9 CFU + Lactobacillus rhamnosus 1×10 9 CFU + Lactobacillus paracasei 1×10 9 CFU | RCT; n = 46 người lớn | Thay đổi độ xơ hóa bằng đo độ đàn hồi gan | Brazil | NCT03467282 |
| NAFLD | 1x men vi sinh/ngày: Lactobacillus acidophilus 10 9 , B. lactis 10 9 | RCT; n = 58 người lớn | Những thay đổi ở gan dựa trên xét nghiệm FIBROMAX | Brazil | NCT02764047 |
| NAFLD | Synbiotic: Fructo-oligosacarit có mức độ trùng hợp ≪10 ở mức 4 g/hai lần một ngày cộng với Bifidobacteria Animalis subsp. lactis BB-12 tối thiểu 10 tỷ CFU/ngày (1 viên mỗi ngày). | RCT; n = 100 người lớn | Thay đổi mỡ gan do MRS | Vương quốc Anh | NCT01680640 |
| NAFLD | 2 lần prebiotic/ngày: inulin giàu oligofructose (Synergy1) | RCT; n = 60 người lớn | Thay đổi mỡ gan bằng MRI, thay đổi xơ hóa gan bằng FibroScan, thay đổi tổn thương gan bằng Fibrotest Score | Canada | NCT02568605 |
| NAFLD | Prebiotic 16 g/ngày: inulin và oligofructose | RCT; n = 60 người lớn | Thay đổi mỡ gan do MRS, sinh hóa | Người israel | NCT02642172 |
| Viêm gan do rượu cấp tính | 1x men vi sinh/ngày: Lactobacillus rhamnosus GG | RCT; n = 130 người lớn | Điểm MELD | nước Mỹ | NCT01922895 |
CFU, đơn vị hình thành thuộc địa; MRS, quang phổ cộng hưởng từ; MRI, chụp cộng hưởng từ; NAFLD, bệnh gan nhiễm mỡ không do rượu; RCT, thử nghiệm ngẫu nhiên có kiểm soát.
Cấy ghép vi sinh vật trong phân
FMT gần đây đã trở thành tiêu chuẩn chăm sóc để điều trị vi khuẩn Clostridium difficil e kháng kháng sinh. Do đó, FMT thường xuyên được nghiên cứu như một lựa chọn điều trị tiềm năng cho nhiều loại bệnh, bao gồm cả những bệnh liên quan đến gan. Như đã nêu trước đây, trục gan-ruột đóng một vai trò thiết yếu trong sinh bệnh học của bệnh gan, với nghiên cứu gần đây cho thấy FMT có thể có lợi.
Một nghiên cứu thí điểm, điều tra tác động của FMT ở 8 bệnh nhân nam bị viêm gan do rượu nặng so với các biện pháp kiểm soát trước đây cho thấy bệnh gan có sự cải thiện rõ rệt trong vòng 1 tuần. Điều này bao gồm việc giải quyết tình trạng cổ trướng và bệnh não gan ở phần lớn bệnh nhân. Họ cũng nhận thấy tỷ lệ sống sót sau 1 năm được cải thiện đáng kể so với nhóm đối chứng phù hợp nhận được tiêu chuẩn chăm sóc (87,5% so với 33,3%). Một thử nghiệm lâm sàng gần đây điều tra xem liệu FMT có cải thiện bệnh não gan so với tiêu chuẩn chăm sóc ở bệnh nhân nam bị xơ gan và bệnh não gan tái phát hay không, cho thấy những người dùng FMT đã giảm tỷ lệ nhập viện và cải thiện nhận thức cũng như rối loạn sinh lý.
Hơn nữa, trong 5 tháng sau thủ thuật FMT, không có người nhận FMT nào phát triển bệnh não gan, trong khi 5 người trong số những người được chăm sóc tiêu chuẩn thì có. Liên quan đến NAFLD, 1 nghiên cứu thí điểm đã báo cáo rằng FMT làm giảm đáng kể tình trạng kháng insulin liên quan đến những thay đổi trong IM. Một lần nữa, cần có nhiều thử nghiệm lâm sàng hơn để điều tra đầy đủ các tác dụng có lợi của FMT đối với các bệnh gan cụ thể, một số trong đó đang được tiến hành (Bảng 3).
Bảng 3
Các thử nghiệm cấy ghép microbiota trong phân hiện nay.
| Loại bệnh gan | Loại cấy ghép vi sinh vật trong phân | Thiết kế nghiên cứu | Kết quả chính | Vị trí |
| NASH | Phân đông lạnh từ người hiến tặng khỏe mạnh gầy được truyền vào tá tràng bằng nội soi | Mở một nhãn hiệu; n = 5 người lớn | Thay đổi mỡ gan bằng MRI | nước Mỹ |
| Xơ gan liên quan đến NASH | Người nhận sẽ nhận được mẫu phân của người hiến tặng khỏe mạnh qua ống thông mũi dạ dày, 100 ml mỗi tháng một lần trong 5 tháng. | RCT; n = 60 người lớn | Giảm chênh lệch áp lực tĩnh mạch gan | Ấn Độ |
| Viêm gan do rượu | FMT của người hiến tặng khỏe mạnh được quản lý bằng ống thông mũi dạ dày trong 7 ngày | RCT; n = 130 người lớn | Tỷ lệ người tham gia sống sót chung sau 3 tháng | Ấn Độ |
| Xơ gan | FMT bằng nội soi và/hoặc thuốc xổ | RCT; n = 60 người lớn | Số lượng tai biến tỷ lệ biến chứng | Trung Quốc |
| Xơ gan | FMT (200 ml) từ các mẫu khỏe mạnh được hiến tặng sẽ được đưa vào tá tràng thông qua nội soi dạ dày | RCT; n = 32 người lớn | Đánh giá tính khả thi của FMT và đánh giá tỷ lệ các tác dụng phụ xảy ra khi điều trị | Vương quốc Anh |
| Xơ gan | Một liều 90 ml thuốc xổ FMT từ mẫu phân của người hiến tặng khỏe mạnh | RCT; n = 20 người lớn | Tỷ lệ người tham gia gặp biến cố bất lợi nghiêm trọng liên quan, mắc các bệnh truyền nhiễm lây truyền mới mắc phải và biến cố bất lợi liên quan | nước Mỹ |
| Bệnh não gan | FMT của người hiến tặng khỏe mạnh nhãn mở một cánh tay được thực hiện ở Tuần 0 bằng nội soi và ở Tuần 1-4 bằng thuốc xổ | Mở một nhãn hiệu; n = 10 người lớn | Thời điểm bệnh não gan bùng phát | Canada |
| Bệnh não gan | Thử nghiệm nhãn mở một trung tâm đối với RBX2660 (hệ thống treo microbiota). FMT của người hiến tặng khỏe mạnh được thực hiện ở Tuần 0 bằng nội soi và ở Tuần 1-4 bằng thuốc xổ | Mở một nhãn hiệu; n = 30 người lớn | Thời điểm bệnh não gan bùng phát | Canada |
| Bệnh não gan | Đối tượng sẽ nhận được 15 viên FMT uống vào các ngày 1, 2, 7, 14 và 21. FMT được điều chế từ những người hiến tặng khỏe mạnh. | RCT; n = 30 người lớn | Điểm bệnh não gan tâm lý | nước Mỹ |
| Suy gan cấp tính | FMT được quản lý bằng thuốc xổ | RCT; n = 40 người lớn | Sống sót | Ấn Độ |
FMT, cấy ghép vi sinh vật trong phân; MRI, chụp cộng hưởng từ; NAFLD, bệnh gan nhiễm mỡ không do rượu; RCT, thử nghiệm ngẫu nhiên có kiểm soát.
Phần kết luận
Có bằng chứng về mối liên quan giữa rối loạn sinh học và bệnh gan, đặc biệt là liên quan đến NAFLD, ALD, xơ gan và bệnh não gan. Cụ thể, các phân tử do IM tạo ra như nội độc tố và các cytokine tiền viêm đóng vai trò trong cơ chế bệnh sinh của bệnh gan. Hơn nữa, IM có thể bị ảnh hưởng bởi một số yếu tố môi trường, đặc biệt là chế độ ăn uống và rượu trong trường hợp NAFLD và ALD.
Ngoài những thay đổi về chế độ ăn uống hoặc kiêng rượu, việc vận dụng IM bằng nhiều biện pháp can thiệp khác nhau cho thấy nhiều hứa hẹn. Phần lớn các nghiên cứu điều tra việc sử dụng pre-, pro- và synbiotic trong NAFLD, ALD và xơ gan/HE và đã phát hiện ra rằng những sản phẩm này cải thiện các dấu hiệu lâm sàng và sinh hóa của bệnh gan, tuy nhiên vẫn còn thiếu các nghiên cứu ở bệnh nhân mắc PSC và PBC.
Tóm lại, mặc dù những nghiên cứu này cho thấy nhiều hứa hẹn nhưng vẫn cần nhiều nghiên cứu lâm sàng hơn, đặc biệt là các thử nghiệm ngẫu nhiên có đối chứng lớn hơn để thu hẹp khoảng cách giữa dữ liệu thực nghiệm/tiền lâm sàng và lượng nhỏ dữ liệu của con người về chủ đề này.